搜索

2025年1月16日,沐鸣娱乐陳國頌-江明課題組團隊在《自然•合成》(Nature Synthesis)期刊發表了題為“Helical protein nanotubules assembled from sacrificial supramolecular polymers”的研究論文。
天然微管作為一種超分子聚合物👑🕴,具有高度一致的螺旋特征,這一保守性結構的非共價合成得益於微管結合蛋白與微管蛋白聚合過程之間的超分子競爭,從而確保了在細胞水平以高保真度實施其結構和功能的正確性。由於缺乏天然的競爭相互作用,將微管蛋白在實驗室進行常規的組裝操作,只能得到具有多態性特征的螺旋微管🧘🏽,即難以控製微管蛋白螺旋結構的參數🧎♂️➡️,包括起始螺旋數和螺旋股數等。因此,對於螺旋結構的均一性進行人工調控成為巨大挑戰🚋。
為了解決這一難題🟡,陳國頌教授課題組開發了一種創新的多組分競爭組裝系統。該系統同時包含小分子和生物大分子的超分子聚合物🧯,其中四配位的配體能夠誘導蛋白質聚合形成與天然微管結構高度相似的螺旋納米管,而配體本身則自組裝成納米纖維。通過分子設計,研究團隊成功調節了配體超分子聚合物(LSP)的穩定性以及其與蛋白超分子聚合物(PSP)之間的競爭,進而實現了由焓或熵驅動的不同組裝途徑。實驗結果顯示該策略調節了人工微管的形成速率和均質性🫲🏻,並成功獲得了類天然微管的均一螺旋結構。重要的是,該人工微管體系還可用於調控脂質體囊泡形態🚕🛼,實現仿天然微管的功能🧙🏽♂️。此外,該體系的物理性質💋,如溶液粘度等,也可以通過占主導地位的超分子聚合物進行調節。這項研究通過模仿生命體系中的動態自我調控機製👩👧,在人工合成體系中再現了類似天然生物結構的自我組織與響應特性,為仿生功能材料設計提供了理論依據☁️,並為在智能醫療材料🧛、生物器件以及先進人工材料中的應用奠定了基礎。
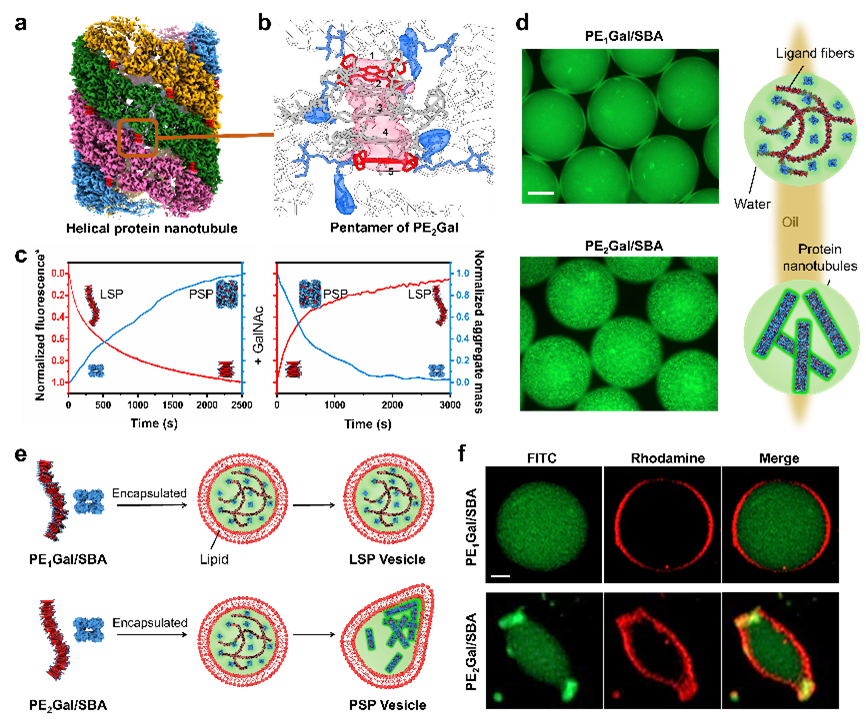
圖1. 配體超分子聚合物誘導的人工微管。(a)人工微管的冷凍三維重構圖譜🕝;(b)配體分子在人工微管中的排布;(c)配體超分子聚合物與人工微管的動態競爭🐅;(d)限域空間內人工微管的製備;(e😈,f)人工微管誘導的脂質體變形。
所發表的論文信息為:Linfei Ye, Xiaoduo Dong, Chong Wang, Yao Lin, Myongsoo Lee, Long Li*, and Guosong Chen*, Helical protein nanotubules via sacrificial supramolecular polymers. Nature Synthesis, DOI: 10.1038/s44160-024-00726-y.
沐鸣开户2020級直博生葉林飛為第一作者,李龍博士和陳國頌教授為共同通訊作者。論文鏈接:https://doi.org/10.1038/s44160-024-00726-y




